
Die Geschwindigkeit chemischer Reaktionen
Datum: 23.01.2013
Beispiele
langsam: Korrision von Eisen
schnell: Verbrennung von Magnesium oder Kohlenstaub
sehr schnell: Knallgasreaktion, Verbrennung eines Benzin-Luft-Gemisches
Wie die Beispiele zeigen, laufen chemische Reaktionen mit sehr unterschiedlichen Geschwindigkeiten ab. Um die Reaktionsgeschwindigkeit
als Größe anwenden zu können wird sie als nächstes gemessen und definiert.
Messung und Definition der chemischen Reaktionsgeschwindigkeit
Geräte und Chemikalien:
Tropftrichter, Rundkolben, Kolbenprober, Salzsäure, Zink
Versuchsaufbau:



Versuchsdurchführung:
Man dreht das Ventil des Tropftrichters auf und liest die Werte des entstehenden Gasvolumens auf dem Kolbenprober in bestimmten Zeitintervallen ab.
Versuchsbeobachtungen:
Es findet eine starke Gasentwicklung statt, die mit der Zeit schwächer wird. Der Kolben fährt aus dem Kolbenprober.
Versuchsvideo Salzsäure mit Zink
Messwerte:
| t/s | 0 | 5 | 10 | 15 | 20 | 25 | 30 | 35 | 40 | 45 | 50 | 55 | 60 |
| V/ml | 0 | 96 | 102 | 108 | 112 | 117 | 120 | 122 | 124 | 125 | 126 | 128 | 129,5 |
| 65 | 70 | 75 | 80 | 85 | 90 | 95 | 100 | 105 | 110 | 115 | 120 | 131 | 132 | 132 | 133 | 134 | 134,5 | 135 | 135,5 | 136 | 136,5 | 136,5 | 136,5 |
Versuchserklärung:
Bei der Reaktion von Zink und Salzsäure entsteht Wasserstoff, dieser wird in dem Kolbenprober aufgefangen.
Anhand des gemessenen Volumens des entstehenden Gases, in Zusammenhang mit der gemessenen Zeit,
kann man mit Hilfe folgender Formel die Reaktionsgeschwindigkeit v ausrechnen:
Mit dieser Formel lässt sich die Durchschnittsgeschwindigkeit im Zeitintervall Δt berechnen.
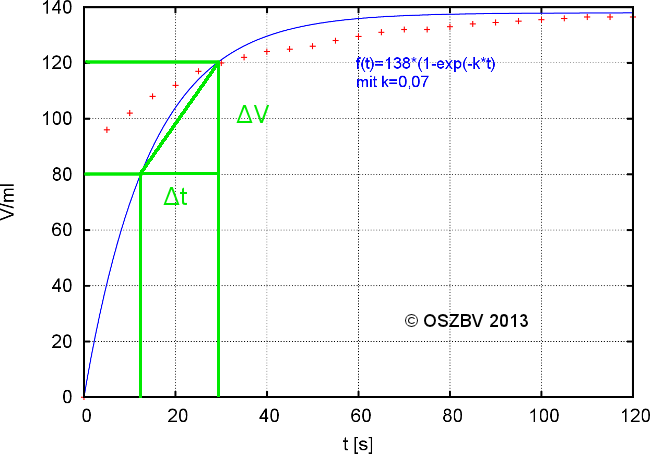
Diagramm mit eingezeichneten Messwerten und der Ausgleichskurve
Die Ausgleichskurve deckt sich leider nicht so gut mit den Messwerten, was an der sehr starken Volumenänderung am Anfang des Experiments lag. Der Kolbenprober bewegte sich auch nicht ruckelfrei. Dadurch entstanden z.T. große Messfehler.
Beispiel:
Mit den Werten aus der Grafik für die Zeit t2=29s und t1=13s und für die Volumina V2=120ml und V1=80ml ergibt sich im eingezeichneten Intervall Δt folgende Durchschnittsgeschwindigkeit:
Versuchsergebnis:
Mit Hilfe der obigen Formeln kann man die Reaktionsgeschwindigkeit einer chemischen Reaktion in einem Intervall berechnen.
Außerdem erkennt man am Verlauf der Ausgleichskurve den exponentiellen Charakter der Volumenänderung. Analog gilt das auch für den
Verlauf der Konzentration:
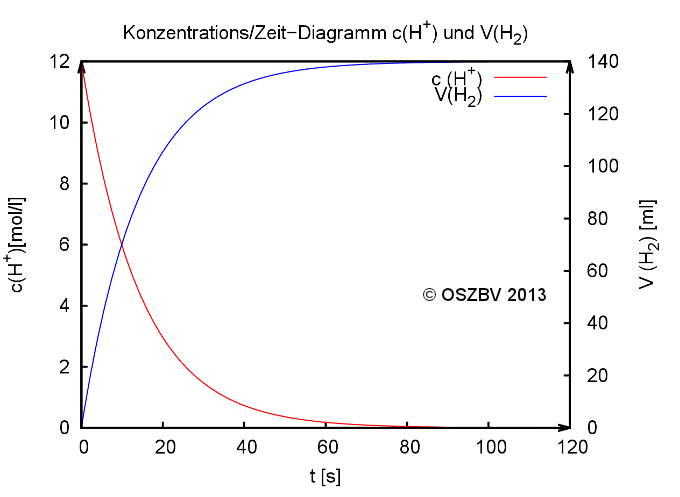
Konzentrations-Zeit-Diagramm und Volumen-Zeitdiagramm der Reaktion
Für die Konzentration der Edukte in Abhängigkeit von der Zeit gilt:
und für die Konzentration der Produkte gilt:
Dazu gibt es auch eine Aufgabe in den Übungsaufgaben zur Klausur.
Einige Texte erstellt von Noah S. mit Ergänzungen durch Herrn Ecker.